Pokud jde o vliv nanomateriálů na lidské zdraví, jsme stále teprve na začátku. K jejich testování se používají pokusná zvířata, s čímž se pojí řada problémů. Alespoň částečné řešení nabízejí uměle vypěstované lidské miniplíce.
Vědci britské University of Manchester pro účel testování vlivu nanomateriálů a dalších faktorů na lidský organismus vypěstovali miniplíce, které se mohou stát užitečnou alternativou k testování na zvířatech. Jak uvádí vedoucí výzkumu buněčná bioložka a nanotoxikoložka Sandra Vranicová, lidské organoidy sice ještě úplně pokusná zvířata nenahradí, jejich používání by ale mělo brzy vést k podstatnému omezení využívání pokusů na zvířatech.
Lidské miniplíce jsou vypěstovány z lidských kmenových buněk v laboratorních podmínkách. Představují mnohobuněčné 3D struktury, které napodobují klíčové charakteristiky lidských tkání, včetně jejich buněčné komplexity a architektury. V současné době se podobné miniplíce čím dál častěji používají při studiu rozmanitých onemocnění plic, od cystické fibrózy přes nádory plic až po plicní infekce včetně SARS-CoV-2.
Vranicová a její kolegové vyvinuli metodu pro přesné dávkování a aplikace nanomater iálů založených na uhlíku pro testování s miniplícemi. Tento postup umožňuje simulovat vliv těchto nanomateriálů na skutečné lidské plíce. V současnosti připravují nový typ miniplic, které obsahuje i lidské buňky imunity.
Dřívější výzkum na zvířecích modelech ukázal, že například dlouhé a pevné mnohostěnné uhlíkové nanostrubičky (MWCNT — multi-walled carbon nanotube) mohou vyvolat chronické záněty a fibrózu plicní tkáně. Testy s lidskými miniplícemi týmu Vranicové odhalily podobnou biologickou odpověď, což potvrzuje jejich použitelnost pro výzkum vlivu nanomateriálů na buněčné úrovni.
Profesor Kostas Kostarelos, předseda nanomedicíny na univerzitě, uvedl, že k dispozici kromě testování na zvířatech je ještě také 2D testování nanomateriálů pomocí dvourozměrných modelů buněčných kultur, jež poskytuje určité pochopení buněčných efektů. Jde však o metodu natolik zjednodušující, že může pouze částečně znázornit komplexní způsob komunikace buněk navzájem, a rozhodně nepostihuje složitost lidského plicního epitelu. Může tedy toxický potenciál nanomateriálů v dobrém i ve zlém podstatně zkreslovat.
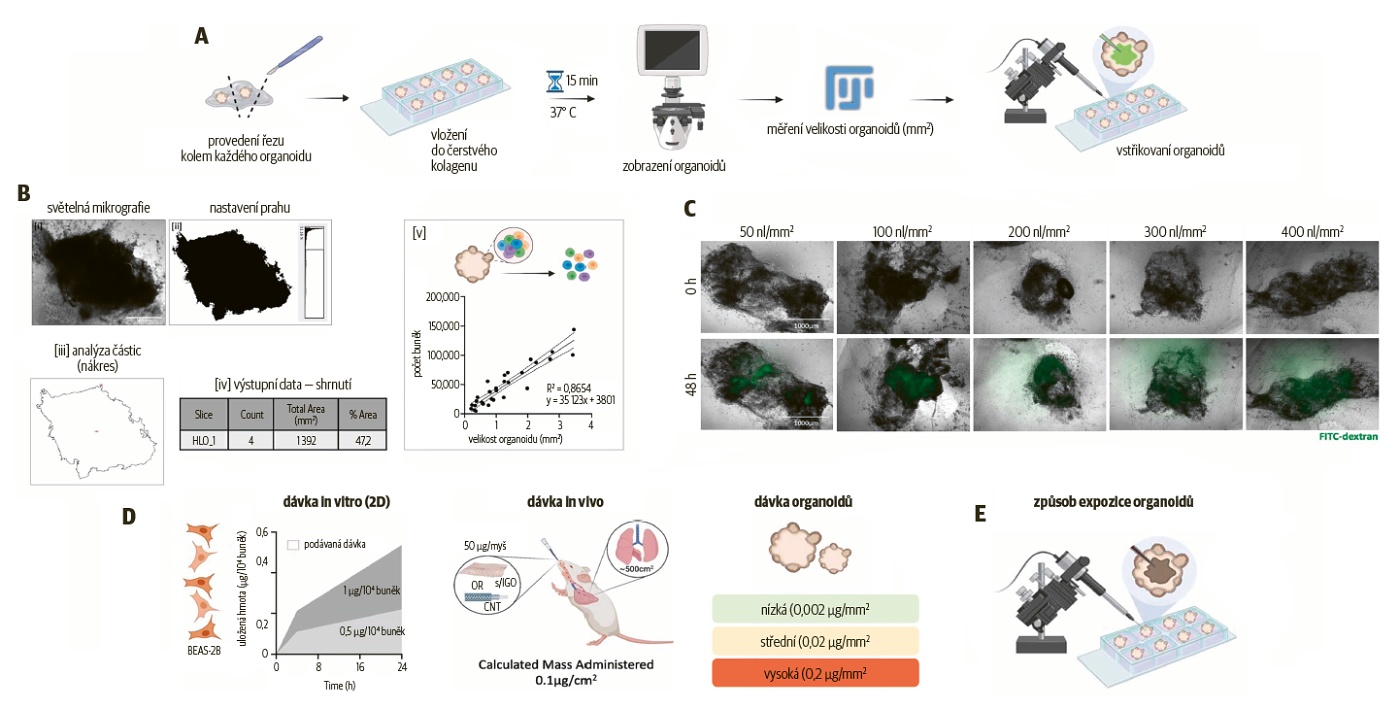
Mikroinjekce lidských plicních organoidů:
- A - experimentální uspořádání pro dodání nákladu do plicních organoidů,
- B - korelace mezi velikostí organoidů (B),
- (C, měřítko 1 000 μm) - měřeno pomocí softwaru pro analýzu obrazu FiJi [i—iv]) a celkovým počtem buněk [v] poté, co jsou organoidy disociovány na jednotlivé buňky, měřítko 500 μm; mikroinjekce různých objemů FITC-dextranu do plicních organoidů před (0 h) a po (48 h) injekci. Oba panely zobrazují události pod filtrem GFP sloučené s jasným polem, n = 2 organoidy na podmínku,
- D - hmotnostní depozice hlášená in vitro pro sGO na lidských plicních epiteliálních buňkách po 24 hodinách expozic,
- E - organoidy byly mikroinjektovány sGO, lGO nebo MWC NT a vystaveny materiálům po dobu 1 den a 7 dní. Dopad expozice materiálu na plicní organoidy byl hodnocen zkoumáním klíčových biologických koncových bodů relevantních pro plicní toxicitu NM na bázi uhlíku, které zahrnovaly cytotoxicitu, interakci materiál-buňka, přestavbu tkáně a plicní fibrózu.